রাসায়নিক গতিবিদ্যা – পর্ব ০২

রসায়নের যে শাখায় রাসায়নিক বিক্রিয়ার বিক্রিয়া হার বা বেগ , বিক্রিয়ার গতিপথ বা ক্রিয়াকৌশল এবং বিক্রিয়া হারের উপর বিভিন্ন প্রভাবকারী বিষয় সম্বন্ধে আলোচনা করা হয়, তাকে রাসায়নিক গতিবিদ্যা (Chemical Kinetics) বলে।
কোনো বিক্রিয়া সংঘটিত হওয়ার সম্ভবনা থাকলেও বিক্রিয়াটি কেন ঘটে না বা কেন ধীর গতিতে সংঘটিত হয়, তার উত্তর রাসায়নিক গতিবিদ্যা থেকে পাওয়া যায়।
রাসায়নিক গতিবিদ্যার সাহায্যে শিল্পে কোনো রাসায়নিক বিক্রিয়া কী হারে সম্পন্ন করলে বিক্রিয়াটি অর্থনৈতিকভাবে লাভজনক হবে তা জানা যায়। এছাড়া বিভিন্ন খাদ্যদ্রব্যের পচন শুরু হতে বা আমাদের দেহে কোনো ওষুধের ক্রিয়া শুরু হতে কত সময় লাগে তাও রাসায়নিক গতিবিদ্যা (Chemical Kinetics) থেকে জানা যায়।
রাসায়নিক গতিবিদ্যা এর কিছু গুরুত্বপূর্ণ প্রশ্ম ও তার উত্তর নিচে দেওয়া হল।
Important Questions and Answers – গুরুত্বপূর্ণ প্রশ্ন ও উত্তর
রাসায়নিক বিক্রিয়ার হার কাকে বলে? তাৎক্ষনিক বিক্রিয়া হার কাকে বলে?
উঃ- প্রতি একক সময়ে কোনো রাসায়নিক বিক্রিয়ায় যে পরিমান বিক্রিয়াজাত পদার্থ উৎপন্ন হয় বা যে পরিমান বিক্রিয়ক পদার্থ অন্তর্হিত হয়, তাকে উক্ত রাসায়নিক বিক্রিয়ার হার বলে।
কোনো রাসায়নিক বিক্রিয়া চলাকালীন কোনো মুহূর্তে কোনো একটি বিক্রিয়ক পদার্থের গাড়ত্ব হ্রাস বা কোনো একটি বিক্রিয়াজাত পদার্থের গাড়ত্ব বৃদ্ধির হারকে ঐ মুহূর্তে বিক্রিয়াটির তাৎক্ষণিক বিক্রিয়া হার বলে।
ভরক্রিয়ার সূত্রটি লেখো।
উঃ- স্থির উষ্ণতায় কোনো রাসায়নিক বিক্রিয়ার কোনো নির্দিষ্ট মুহূর্তে বিক্রিয়া -হার, বিক্রিয়ার শমিত সমীকরণ অনুযায়ী অণু সংখ্যার ঘাতে উন্নিত বিক্রিয়ক গুলির সেই মুহূর্তের সক্রিয় ভরের সমানুপাতিক।
ধরি, কোনো রাসায়নিক বিক্রিয়া, aA + bB → P
ভরক্রিয়ার সূত্র অনিযায়ী, বিক্রিয়া হার (r) ∝ [A]a[B]b
রাসায়নিক বিক্রিয়ার ক্রম ও অণবিকতা বলতে কি বোঝ?
উঃ- ক্রমঃ বিক্রিয়া হার সমীকরণে বিক্রিয়ক গুলির গাড়ত্বের ঘাত সমূহের সমষ্টিকে বিক্রিয়াটির ক্রম বলে।
আণবিকতাঃ একটি মৌলিক বিক্রিয়া সংঘটিত হওয়ার জন্য সর্বনিন্ম যতগুলি বিক্রিয়ক কণার (অণু, পরমাণু বা আয়ন ) প্রয়োজন, সেই সংখ্যাকে উক্ত বিক্রিয়াটির আণবিকতা বলে।
ক্রম ও আণবিকতার মধ্যে পার্থক্য লেখো।
উঃ-
| ক্রম | আণবিকতা |
| i) হার নির্দেশক সমীকরণের ঘাতের সমষ্টিকে বোঝায়। |
i) মৌলিক বিক্রিয়া সংঘটিত হওয়ার জন্য সর্বনিন্ম যতগুলি অণু, পরমানু বা আয়ন প্রয়োজন তাকে বোঝায়। |
| ii) ক্রম শূন্য , পূর্ণ সংখ্যা বা ভগ্নাংশ হতে পারে। | ii) আণবিকতা সবসময় পূর্ণ সংখ্যা হয়। |
| iii) গাড়ত্ব , উষ্ণতা ও চাপের পরিবর্তনে ক্রমের পরিবর্তন হয় না । |
iii) আণবিকতার মান গাড়ত্ব , উষ্ণতা ও চাপের ওপর নির্ভর করে। |
| iv) এটি একটি পরীক্ষা লব্ধ রাশি । | iv) এটি একটি তাত্বিক রাশি। |
শূন্য ক্রম , প্রথম ক্রম, দ্বিতীয় ক্রম, তৃতীয় ক্রম ও ভগ্নাংশ ক্রম বিক্রিয়ার উদাহরণ দাও ।
উঃ- শূন্য ক্রম বিক্রিয়াঃ- যেসব বিক্রিয়ার বিক্রিয়া হার বিক্রিয়কের গাড়ত্বের ওপর নির্ভরশীল নয়, তাদের শূন্য ক্রম বিক্রিয়া বলে। উদাহরণ-
বিক্রিয়া হার = k[HI]0
প্রথম ক্রম বিক্রিয়াঃ- যেসব বিক্রিয়ার বিক্রিয়া হার বিক্রিয়কের গাড়ত্বের প্রথম ঘাতের সমানুপাতিক তাদের প্রথম ক্রম বিক্রিয়া বলে। উদাহরণ-
বিক্রিয়া হার = k[N2O5]
দ্বিতীয় ক্রম বিক্রিয়াঃ- যেসব বিক্রিয়ার বিক্রিয়া হার বিক্রিয়কের গাড়ত্বের দ্বিতীয় ঘাতের সমানুপাতিক তাদের দ্বিতীয় ক্রম বিক্রিয়া বলে। উদাহরণ-
বিক্রিয়া হার = k[NO][O3]
তৃতীয় ক্রম বিক্রিয়াঃ- যেসব বিক্রিয়ার বিক্রিয়া হার বিক্রিয়কের গাড়ত্বের দ্বিতীয় ঘাতের সমানুপাতিক তাদের তৃতীয় ক্রম বিক্রিয়া বলে। উদাহরণ-
বিক্রিয়া হার = k[NO2]2[O2]
ভগ্নাংশ ক্রম বিক্রিয়া:- যেসব বিক্রিয়ার হার নির্দেশক সমীকরণে বিক্রিয়কের গাড়ত্বের ঘাত ভগ্নাংশ তাদের ভগ্নাংশ ক্রম বিক্রিয়া বলে। উদাহরণ-
বিক্রিয়া হার = k[CH3CHO]3/2
শূন্য ক্রম , প্রথম ক্রম, দ্বিতীয় ক্রম বিক্রিয়ার হার ধ্রুবকের একক নির্ণয় করো।
উঃ- r = k [A]n
বিক্রিয়া হার (r)= গাড়ত্ব/সময়
= mol.L-1 / s = mol. L-1. s-1
k = r / [A]n
= mol.L-1.s-1 / (mol.L-1)n
= (mol.L-1)1-n. s-1
শূন্য ক্রমের ক্ষেত্রে (n=0), k= mol.L-1.s-1
প্রথম ক্রমের ক্ষেত্রে (n=1), k= s-1
দ্বিতীয় ক্রমের ক্ষেত্রে (n=2), k= (mol.L-1)-1.s-1
শূন্য ক্রম বিক্রিয়ার ক্ষেত্রে হার নির্দেশক সমীকরণ প্রতিষ্ঠা করো।
উঃ- ধরি, একটি শূন্য ক্রম বিক্রিয়া
A → B
প্রাথমিক অবস্থায় [A]=a, সাম্যবস্থায়, [A]=(a-x)
বিক্রিয়া হার,
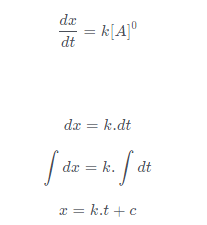
যখন t = 0, তখন x = 0, অর্থাৎ c = 0
অতএব, x = k.t
শূন্য ক্রম বিক্রিয়ার ক্ষেত্রে হার নির্দেশক সমীকরণ x = k.t
শূন্য ক্রম বিক্রিয়ার অর্ধায়ু নির্ণয়ের সমীকরণ প্রতিষ্ঠা করো। অথবা, একটি শূন্য ক্রম বিক্রিয়ায় দেখাও যে, বিক্রিয়ার প্রারম্ভিক গাড়ত্বের সঙ্গে অর্ধায়ু সমানুপাতিক।
উঃ- শূন্য ক্রম বিক্রিয়ার হার নির্দেশক সমীকরণ,
x = k.t
বা, t = x/k
যখন অর্ধায়ু হয় তখন t = t1/2 এবং x= a/2 হয়।
অতএব, t1/2 = a/2k
অর্থাৎ, শূন্য ক্রম বিক্রিয়ার ক্ষেত্রে বিক্রিয়ার প্রারম্ভিক গাড়ত্বের সঙ্গে অর্ধায়ু সমানুপাতিক হয়।
t1/2 ∞ a
প্রথম ক্রম বিক্রিয়ার ক্ষেত্রে হার নির্দেশক সমীকরণ প্রতিষ্ঠা করো।
উঃ- ধরি, একটি প্রথম ক্রমের বিক্রিয়া,
A → B
প্রাথমিক অবস্থায় [A]=a, সাম্যবস্থায়, [A]=(a-x)
প্রথম ক্রম বিক্রিয়ার হার, dx/dt = k.[A]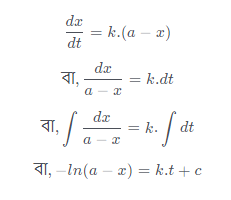
যখন হয় t = 0 হয়, তখন x = 0 হয়, অর্থাৎ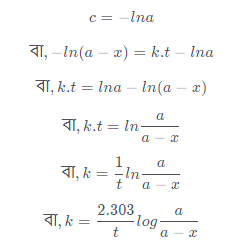
প্রথম ক্রম বিক্রিয়ার অর্ধায়ু বলতে কি বোঝো।
উঃ- কোনো প্রথম ক্রম বিক্রিয়া চলাকালীন যে সময়ে বিক্রিয়কের গাড়ত্ব সেটির প্রাথমিক গাড়ত্বের অর্ধেক হয়, তাকে প্রথম ক্রম বিক্রিয়ার অর্ধায়ু বা অর্ধজীবনকাল বলে।
দেখাও যে, প্রথম ক্রম বিক্রিয়ার অর্ধায়ু প্রারম্ভিক গাড়ত্বের ওপর নির্ভর করে না। অথবা, প্রথম ক্রম বিক্রিয়ার অর্ধায়ু এবং হার ধ্রুবকের মধ্যে সম্পর্ক নির্ণয় করো।
উঃ- প্রথম ক্রম বিক্রিয়ার হার নির্দেশক সমীকরণ,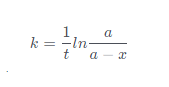
প্রথম ক্রম বিক্রিয়ার ক্ষেত্রে যখন অর্ধায়ু হয় তখন t = t1/2 হয় এবং x = a/2 হয়। অতএব,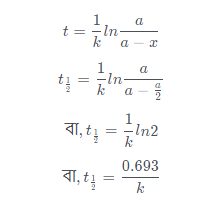
প্রথম ক্রম বিক্রিয়ার অর্ধায় নির্ণয়ের সমীকরণে প্রাথমিক গাড়ত্ব সংক্রান্ত কোনো রাশি না থাকায় বলা যায় প্রথম ক্রম বিক্রিয়ার অর্ধায়ু প্রাথমিক গাড়ত্বের ওপর নির্ভর করে না।
ছদ্ম প্রথম ক্রম বিক্রিয়া কাকে বলে ? উদাহরণ দাও ।
উঃ- অনেক রাসায়নিক বিক্রিয়া আছে যাদের ক্ষেত্রে একাধিক বিকারক রাসায়নিক বিক্রিয়ায় অংশ গ্রহণ করলেও বিক্রিয়ার হার শুধুমাত্র একটি বিকারকের গাড়ত্বের ওপর নির্ভর করে এবং বিকারকটির সাপেক্ষে বিক্রিয়াটি প্রথম ক্রমের হয়। এই ধরনের বিক্রিয়াকে ছদ্ম প্রথম ক্রমের বিক্রিয়া বলে।
উদাহরণ- C12H22O11 + H2O → C6H12O6 + C6H12O6
দেখাও যে, প্রথম ক্রম বিক্রিয়া কখনই সম্পূর্ণ হয় না।
উঃ- প্রথম ক্রম বিক্রিয়ার হার নির্দেশক সমীকরণ,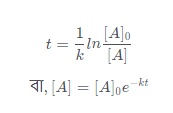
যেখানে [A]0 ও [A] যথাক্রমে বিক্রিয়ার শুরুতে (t= 0 সময়ে) এবং বিক্রিয়া শুরু হওয়ার t সময় পরে বিক্রিয়কের গাড়ত্ব।
বিক্রিয়াটি যখন সম্পূর্ণ হবে তখন বিক্রিয়কের গাড়ত্বের মান অর্থাৎ [A] এর মান শূন্য হবে।
অতএব, সমীকরণে [A] = 0 বসিয়ে পাই,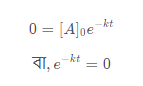
e-kt = 0 হবে যদি t = ∞ হয়। অর্থাৎ, প্রথম ক্রম বিক্রিয়া সম্পূর্ণ হতে অসীম সময় প্রয়োজন।
সুতরাং, বলা যায়, প্রথম ক্রম বিক্রিয়া কখনই সম্পূর্ণ হয় না।
সক্রিয়করন শক্তি কাকে বলে? আরহেনিয়াসের সমীকরণটি লেখো।
উঃ- কোনো বিক্রিয়ায় বিক্রিয়ক পদার্থের অণুগুলি তাদের গড় গতিশক্তির অধিক সর্বনিন্ম যে অতিরিক্ত পরিমান শক্তি অর্জন করলে সক্রিয় হয়ে ওঠে এবং বিক্রিয়া সাধনের উপযুক্ত হয়, তাকে সক্রিয়করন শক্তি বলে।
আরহেনিয়াসের সমীকরণ-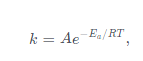
[যেখানে A= কম্পাঙ্ক গুনাঙ্ক, k = হার-ধ্রুবক, Ea = সক্রিয়করন শক্তি, R= সার্বজনীন গ্যাস ধ্রুবক, T = পরম উষ্ণতা]
উষ্ণতা গুনাঙ্ক কী?
উঃ- কোনো রাসায়নিক বিক্রিয়ার প্রতি 10 ডিগ্রী সেলসিয়াস উষ্ণতার ব্যবধানে যে দুটি হার ধ্রুবক পাওয়া যায়, সেই দুটি হার ধ্রুবকের অনুপাতকে ঐ বিক্রিয়ার উষ্ণতা গুনাঙ্ক বলে।
ধরা যাক, ToC উষ্ণতায় কোনো রাসায়নিক বিক্রিয়ার হার KT এবং T (T+10)oC উষ্ণতায় কোনো রাসায়নিক বিক্রিয়ার হার K(T+10) হলে,
উষ্ণতা গুনাঙ্ক= K(T+10) / KT
বেশির ভাগ বিক্রিয়ার ক্ষেত্রে উষ্ণতা গুনাঙ্ক এর মান 2 থেকে 3 এর মধ্যে হয়।
কোনো রাসায়নিক বিক্রিয়ার হার কি কি বিষয়ের ওপর নির্ভর করে?
উঃ-
১) বিক্রিয়ক গুলির গাড়ত্ব
২) বিক্রিয়ক গুলির প্রকৃতি
৩) কঠিন বিক্রিয়কের পৃষ্ঠতলের ক্ষেত্রফল
৪) সিস্টেমের উষ্ণতা
৫) অনুঘটকের উপস্থিতি
একটি বিক্রিয়া শূন্য ক্রমের হলে ওর আণবিকতাও কী শূন্য হবে?
উঃ- না, আণবিকতা কখনোও শূন্য হয় না।
উষ্ণতা বৃদ্ধিতে কোনো রাসায়নিক বিক্রিয়ার হার বৃদ্ধি পায় কেন?
উঃ- সব রাসায়নিক বিক্রিয়ার ক্ষেত্রে উষ্ণতা বৃদ্ধির ফলে বিক্রিয়ার হার বৃদ্ধি পায় এবং উষ্ণতা হ্রাসের ফলে বিক্রিয়ার হার হ্রাস পায়। বিক্রিয়কের উপাদান পরমানুগুলির বন্ধন গুলিকে ভেঙে বিক্রিয়ক পদার্থ গুলির মধ্যে কার্যকরী সংঘর্ষ ঘটাতে বেশি উষ্ণতার প্রয়োজন হয়। এইজন্য রাসায়নিক বিক্রিয়ায় উষ্ণতার প্রভাব বেশি। উষ্ণতার প্রভাবে বিভিন্ন বিক্রিয়ার হার বৃদ্ধি বিভিন্ন কিন্তু সাধারণভাবে প্রতি দশ ডিগ্রী উষ্ণতা বৃদ্ধিতে বিক্রিয়ার হার দ্বিগুণ থেকে তিনগুন হয়ে যায়।
একটি শূন্য ক্রম বিক্রিয়ার t1/2 বনাম [A]0 বিক্রিয়ার প্রাথমিক গাড়ত্বের লেখচিত্র অঙ্কন করো।
উঃ- শূন্য ক্রম বিক্রিয়ার হার নির্দেশক সমীকরণ,
x = k.t
প্রাথমিক গাড়ত্ব [A]0 হলে, x= [A]0/2 এবং t = t1/2 হয়।
অতএব, t1/2 = [A]0 /2k
বা, t1/2 ∞ [A]0
শূন্য ক্রম বিক্রিয়ার অর্ধায়ু (t1/2) প্রাথমিক ([A]0) গাড়ত্বের সমানুপাতিক।

বহু ধাপে সংঘটিত কোনো রাসায়নিক বিক্রিয়ার কোন মৌলিক ধাপটি “হার নির্ণায়ক ধাপ“ হিসাবে গন্য হয়?
উঃ- বহু ধাপে সংঘটিত কোনো রাসায়নিক বিক্রিয়ার সবচেয়ে ধীরগতিসম্পন্ন ধাপকে উক্ত বিক্রিয়ার “হার নির্ণায়ক ধাপ” হিসাবে গন্য করা হয়।
অনুঘটক রাসায়নিক বিক্রিয়ার হার কীভাবে বাড়ায়? স্থির উষ্ণতায় অনুঘটকের উপস্থিতিতে রাসায়নিক বিক্রিয়ার এনথ্যালপি সমান থাকে না অপরিবর্তিত থাকে?
উঃ- অনুঘটক এর উপস্থিতিতে রাসায়নিক বিক্রিয়ার সক্রিয়করণ শক্তি হ্রাস পায়, ফলে বিক্রিয়ার হার বৃদ্ধি পায়।
স্থির উষ্ণতায় অনুঘটকের উপস্থিতিতে বা অনুপস্থিতিতে রাসায়নিক বিক্রিয়ার এনথ্যালপি সমান থাকে।
বিক্রিয়ার সংঘর্ষ তত্ব অনুযায়ী সকল আণব সংঘর্ষই কেন ” কার্যকারী সংঘর্ষে ” রূপান্তরীত হয় না?
উঃ- যেসব সংঘর্ষের ফলে বিক্রিয়ক অণুগুলি সফলভাবে বিক্রিয়া ঘটিয়ে বিক্রিয়াজাত পদার্থে রূপান্তরীত হয়, সেগুলিকে কার্যকারী সংঘর্ষ বলে। কার্যকারী সংঘর্ষ ঘটাতে বিক্রিয়ক অনুগুলিকে দুই প্রকার বাধা অতিক্রম করতে হয়। ১. শক্তিজনিত বাধা; ২. বিন্যাসগত বাধা। এই দুই ধরনের বাধা অতিক্রম করলে তবেই সকল আণব সংঘর্ষ কার্যকারী সংঘর্ষে রূপান্তরীত হয়।
প্রথম ক্রম বিক্রিয়ার হার ধ্রুবকের একক কী?
সময়-1 (S-1, min-1)
বিক্রিয়ার হার ধ্রুবক বলতে কি বোঝ?
উঃ- নির্দিষ্ট উষ্ণতায় একক গারত্ব বিশিষ্ট বিক্রিয়কগুলি দ্বারা সংঘটিত রাসায়নিক বিক্রিয়ার বিক্রিয়া হারকে ওই উষ্ণতায় উক্ত বিক্রিয়ার হার-ধ্রুবক বলে।
একটি বিক্রিয়ার হার ধ্রুবকের একক (mol)-1/2 .(dm)3/2 . s-1 হলে, বিক্রিয়াটির ক্রম কত হবে?
উঃ- আমরা জানি, n- তম বিক্রিয়ার হার ধ্রুবক, k= (mol.L-1)1-n. s-1
অতএব, (mol.L-1)1-n. s-1 = (mol)-1/2 .(dm)3/2 . s-1
বা, (mol.L-1)1-n = (mol-1/2 .L1/2)
বা, (mol.L-1)1-n = (mol .L-1)-1/2
অতএব, (1-n)=-1/2
বা, n=(1+1/2)
বা, n=3/2
বিক্রিয়াটির ক্রম = 3/2
মৌলিক ও জটিল বিক্রিয়া কাকে বলে?
উঃ-
মৌলিক বিক্রিয়াঃ যেসব বিক্রিয়া কেবলমাত্র একটি ধাপেই সম্পন্ন হয় এবং অন্তর্বতী রুপে কোনো জটিল যৌগ গঠন করে না, সেই সমস্ত বিক্রিয়াকে জটিল বিক্রিয়া বলে। উদাহরণ- H2+I2 → 2HI
জটিল বিক্রিয়াঃ যেসব বিক্রিয়া কেবলমাত্র একাধিক ধাপে সম্পন্ন হয় এবং অন্তর্বতী রুপে এক বা একাধিক জটিল যৌগ গঠন করে, সেই সমস্ত বিক্রিয়াকে জটিল বিক্রিয়া বলে। উদাহরণ- 2N2O5 → 4NO2 + O2
অতিমন্থর বিক্রিয়া ও অতিদ্রুত গতির বিক্রিয়ার উদাহরণ দাও।
উঃ-
অতিদ্রুত গতির বিক্রিয়াঃ জলীয় দ্রবণে যেসব বিক্রিয়ায় মৌলের জারণ সংখ্যার কোনো রুপ পরিবর্তন ঘটে না, সেগুলি অতি দ্রুত হারে সংঘটিত হয়। যেমন অ্যাসিড ক্ষার প্রশ্মন বিক্রিয়া HCl + NaOH → NaCl + H2O
অতিমন্থর বিক্রিয়াঃ সাধারণ চাপ ও উষ্ণতায় অনুঘটকের অনুপস্থিতিতে H2 ও O2 গ্যাস-মিশ্রণকে রেখে দিলেও কোনো পরিবর্তন লক্ষ করা যায় না।
একটি প্রথম ক্রম বিক্রিয়ার বেগ ধ্রুবক k এর ভৌত তাৎপর্য কী?
উঃ- কোনো প্রথম ক্রম বিক্রিয়া ঘটার সময় যদি কোনো মুহুর্তে বিক্রিয়কের গাড়ত্ব= [A] হয়, তবে ওই মুহুর্তে বিক্রিয়া-হার, -d[A]/dt = k[A] (যেখানে k = হার-ধ্রুবক)
বা, k = -(d[A]/[A]).(dt)
= বিক্রিয়কের যত ভগ্নাংশ বিক্রিয়াজাত পদার্থে রূপান্তরিত হয় / সময়
সুতরাং, একক সময়ে বিক্রিয়কের যত ভগ্নাংশ বিক্রিয়াজাত পদার্থে রূপান্তরিত হয়েছে তা k এর মান দ্বারা নির্দেশিত হয় (অবশ্য যদি ওই একক সময়ে বিক্রিয়কের গাড়ত্ব অপরিবর্তিত থাকে)।
প্রথম ক্রম বিক্রিয়ার সমাকলিত হার সমীকরণটি লেখো এবং লেখচিত্রের সাহায্যে k এর মান নির্ণয় করো।
উঃ- প্রথম ক্রম বিক্রিয়ার সমাকলিত হার সমীকরণটি হল-
উপরিউক্ত সমীকরণ থেকে পাই,
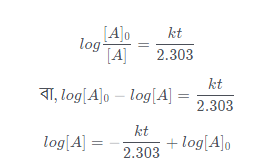
সমীকরণটি একটি সরলরেখার সমীকরণ নির্দেশ করে। সুতরাং, বিক্রিয়া চলাকালীন বিভিন্ন সময়ে (t) বিক্রিয়কের গাড়ত্ব ( [A] ) পরীক্ষার সাহায্যে পরিমাপ করে যদি y অক্ষ বরাবর log[A] এবং x অক্ষ বরাবর t এর মান বসিয়ে লেখচিত্র অঙ্কন করা হয়, তবে ঋণাত্মক নতিযুক্ত একটি সরলরেখা পাওয়া যায়। প্রাপ্ত সমীকরণটির নতির মান থেকে হার- ধ্রুবকের (k) মান নির্ণয় করা যায়।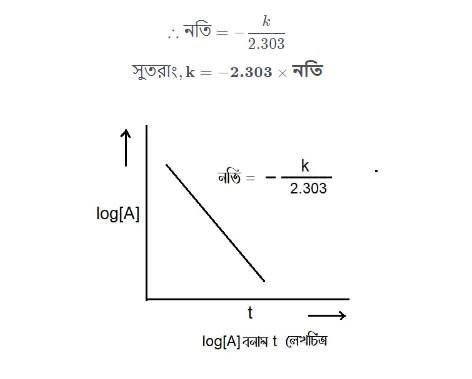
![]()